En combinant les principes de la microfluidique, de la microfabrication et des techniques de culture cellulaire, une nouvelle génération de plateformes de laboratoire a émergé, connue sous le nom d'« organe-sur-puce ». Les systèmes organe-sur-puce sont des dispositifs microfluidiques contenant des cellules vivantes. Ces dispositifs microfluidiques peuvent mieux récapituler les microenvironnements par rapport aux modèles in vitro précédents. Les dispositifs microfluidiques sont particulièrement adaptés à la modélisation des barrières biologiques, telles que la barrière hémato-encéphalique, car ils peuvent modéliser le flux sanguin.
Structure et fonction de la barrière hémato-encéphalique
La barrière hémato-encéphalique (BHE) est la couche limite de cellules qui tapisse les microvaisseaux cérébraux et sépare le sang des fluides interstitiels cérébraux. La fonction principale de la barrière hémato-encéphalique est d'agir comme une barrière physique et métabolique en permettant le transport sélectif des nutriments, mais en empêchant les substances toxiques présentes dans le sang de pénétrer dans le cerveau.
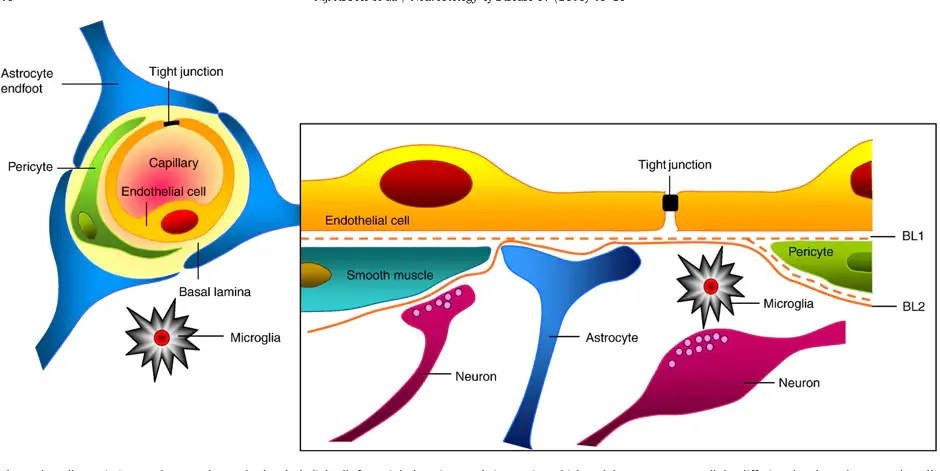
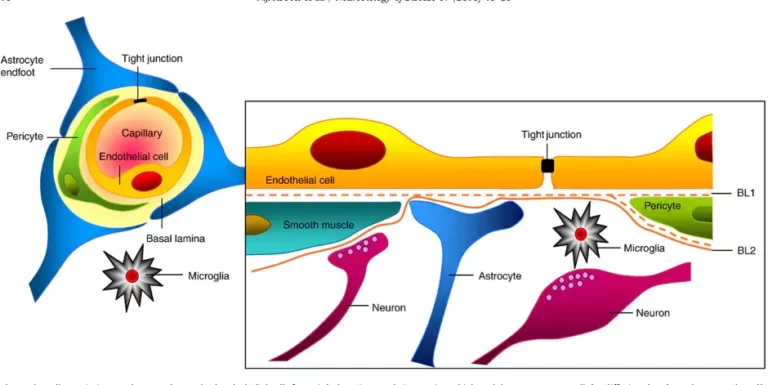
La BHE est composée de cellules endothéliales spécialisées qui sont entourées d'une membrane basale et de quatre autres types de cellules : les astrocytes, les péricytes, les neurones et la microglie. Ces cinq types de cellules et la membrane basale constituent ensemble l'unité neurovasculaire (figure 1) [1]. Des complexes protéiques d'étanchéité appelés jonctions serrées se forment entre les cellules endothéliales adjacentes de la BHE. En conséquence, les cellules sont maintenues en étroite proximité les unes des autres, occluant ainsi les espaces intracellulaires et empêchant le transport paracellulaire. Cette forte étanchéité de la barrière est caractéristique de la BHE et cruciale pour le maintien de l'homéostasie cérébrale. Une perturbation locale de l'étanchéité de la barrière, entraînant une fuite à travers celle-ci, est associée à plusieurs maladies du système nerveux central (SNC) [2]. Comprendre et surmonter la BHE est essentiel pour le traitement des maladies du SNC. Les systèmes d'administration de médicaments qui peuvent temporairement ouvrir la barrière, permettant aux médicaments de passer et d'atteindre le cerveau, constituent un domaine de recherche clé pour le traitement des maladies du SNC.
Modèles in vitro de la barrière hémato-encéphalique
Dans des environnements artificiels, les conditions peuvent être maintenues sous un contrôle strict et des comportements spécifiques peuvent être étudiés indépendamment avec peu d'interférence d'autres facteurs. Traditionnellement, la BHE a été reconstruite in vitro sous forme de modèles statiques utilisant des configurations de culture cellulaire conventionnelles. Les dispositifs microfluidiques organe-sur-puce offrent des solutions à de nombreuses lacunes des modèles in vitro précédents. Ces dispositifs peuvent être conçus avec des architectures plus réalistes et leurs petites dimensions représentent mieux la géométrie des capillaires dans l'unité neurovasculaire. De plus, en employant la microfluidique au lieu de mener des expériences dans une solution en vrac, les modèles peuvent présenter des phénomènes physiologiques tels que les flux de fluides et les contraintes de cisaillement. Un autre avantage des modèles BHE-sur-puce est que des capteurs pour la surveillance en temps réel peuvent être intégrés [3].
Barrière hémato-encéphalique sur une puce microfluidique
Deux des premiers dispositifs microfluidiques qui ont été les pionniers du développement de la BHE-sur-puce et ont fourni des preuves de concept pour plusieurs approches prometteuses sont présentés ci-dessous. Certains aspects importants de conception et paramètres de validation à prendre en compte lors du développement d'un dispositif organe-sur-puce pour étudier la BHE seront également introduits. Aujourd'hui, des puces prêtes à l'emploi pour les applications organe-sur-puce sont disponibles commercialement ou peuvent être commandées sur mesure.
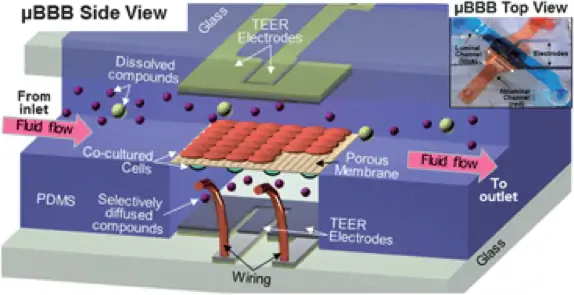
À notre connaissance, Booth et al. ont été les premiers à publier un modèle BHE sur puce en 2012 [4], suivi d'un article en 2014 [5]. Leur dispositif, présenté à la figure 2, comprend deux canaux croisés dans des couches de PDMS, avec une profondeur de 200 µm et une largeur de 2 mm et 5 mm respectivement. Les deux canaux étaient séparés par une membrane de polycarbonate poreuse recouverte de fibronectine. Les couches de canaux étaient recouvertes de lames de verre avec des électrodes Ag/AgCl en couche mince dotées d'une structure de détection à quatre points placée sur la membrane. Des cellules endothéliales de souris (b.End3) et des astrocytes murins (C8D1A) ont été cocultivées sur les côtés opposés de la membrane. Un débit de 2,6 mL/min a été appliqué dans les deux canaux, ce qui, selon les calculs présentés dans l'article, correspondait à une contrainte de cisaillement de 2 mPa sur les cellules endothéliales. La résistance électrique transendothéliale (TEER) a été mesurée entre 180 et 280 Vcm2 avec les électrodes en couche mince intégrées. De plus, la protéine de jonction serrée ZO-1 a été identifiée par immunofluorescence, et des études de perméabilité ont été réalisées pour confirmer la fonction de barrière.
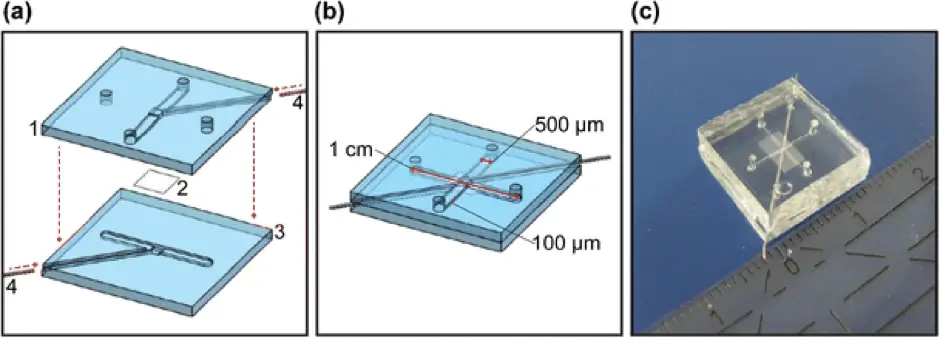
Un autre dispositif BHE entièrement intégré a été publié par Griep et al. en 2013 [6]. Le dispositif était composé de deux couches de PDMS comprenant des canaux d'une largeur de 500 µm et d'une profondeur de 100 µm, avec une membrane de polycarbonate recouverte de collagène intercalée. Des cellules endothéliales microvasculaires cérébrales humaines (hCMEC/D3) ont été cultivées sur la membrane. Ils ont utilisé quatre fils de platine pour surveiller la valeur de TEER sur 7 jours à partir de mesures par spectroscopie d'impédance. Ils ont obtenu une valeur moyenne de TEER de 28 Vcm2 ± 1,3 SEM. Ils ont observé une augmentation de la TEER, jusqu'à 120 Vcm2, lorsqu'un débit de 2,5 mL/h était appliqué, correspondant à une contrainte de cisaillement calculée de 0,58 Pa.
Matériau de la puce pour organe-sur-puce
Le PDMS a été largement utilisé pour fabriquer des dispositifs organe-sur-puce. Parmi les avantages du PDMS, on compte sa biocompatibilité, sa transparence (240 nm – 1100 nm), son faible coût et sa facilité de cadre, sa capacité à être moulé avec une haute résolution, et sa faculté à se lier au verre ou au PDMS [7]. Il est cependant fortement hydrophobe, ce qui peut être problématique lors du remplissage des canaux ou pour obtenir une liaison étanche pour des puces sans fuite. De plus, il est difficile de déposer des électrodes sur la surface du PDMS, et le verre est donc souvent utilisé dans les dispositifs dotés d'électrodes en couches minces structurées.
Cellules dans les modèles de barrière hémato-encéphalique sur puce
Le type de cellules utilisées est d'une grande importance pour construire des modèles de pertinence biologique. Il n'est cependant pas encore clair comment les différentes cellules de l'unité neurovasculaire contribuent précisément à la fonction de barrière [8]. Pour mimer la BHE humaine, l'utilisation de cellules humaines serait évidemment la plus prédictive. Les cellules endothéliales des capillaires cérébraux humains ont été largement caractérisées mais présentent une faible disponibilité et reproductibilité [1]. Les avancées récentes dans la dérivation de cellules souches pluripotentes induites humaines (hiPSC) sont très prometteuses pour surmonter ces difficultés [9].
La co-culture de cellules endothéliales avec d'autres cellules de l'unité neurovasculaire est considérée comme une représentation plus pertinente sur le plan physiologique, car ces cellules influencent également la formation et le maintien de la barrière [10]. Plusieurs études de co-cultures dans des modèles microfluidiques de BBB ont déjà été publiées, principalement des cellules endothéliales avec des astrocytes [4] [11], mais aussi avec des neurones [12] et des péricytes. Les astrocytes et les cellules endothéliales ne sont pas en contact direct l'un avec l'autre mais sont séparés par la lame basale. Dans les dispositifs microfluidiques, elles peuvent être cultivées sur des côtés séparés de la membrane. Cependant, si la membrane du dispositif est trop épaisse, le contact cellule-cellule sera limité. Pour imiter l'environnement 3D de la matrice extracellulaire, des hydrogels ont été utilisés comme échafaudages d'ensemencement cellulaire à l'intérieur des chambres microfluidiques [12].
Contrainte de cisaillement sur les cellules endothéliales
Les cellules endothéliales de la BHE au sein de l'unité neurovasculaire sont soumises à une force normale à la paroi du vaisseau due à la pression sanguine, ainsi qu'à un cisaillement résultant du flux sanguin, dans la direction du flux. Il a déjà été rapporté que les contraintes de cisaillement influencent la morphologie et la fonction des cellules endothéliales, et qu'elles ont un effet positif sur la formation de la barrière [13]. Les dispositifs organe-sur-puce ont le grand avantage d'être adaptés à l'incorporation d'un flux de fluide, contrairement à d'autres types de dispositifs. Les vaisseaux sanguins vivants ont des sections transversales circulaires, tandis que les dispositifs microfluidiques ont généralement des sections transversales rectangulaires. Dans un tube de section transversale circulaire, la contrainte de cisaillement sera égale et uniforme sur les parois en raison de la symétrie cylindrique. Dans le cas d'une section transversale rectangulaire, cependant, la contrainte de cisaillement ne sera pas uniforme. Pour obtenir la contrainte la plus uniforme dans une section transversale rectangulaire, un profil de flux aussi plat que possible peut être réalisé en concevant les canaux de manière à ce que la hauteur du canal soit beaucoup plus petite que la largeur du canal [14]. La contrainte de cisaillement physiologique pour les capillaires cérébraux est de 0,3-2 Pa [2].
Résistance électrique transendothéliale (TEER)
La TEER décrit la résistance à travers une barrière cellulaire et est souvent utilisée comme paramètre de validation pour vérifier si les cellules endothéliales dans les modèles de BHE forment des complexes de jonctions serrées [15]. Si les cellules endothéliales se développent correctement et forment des jonctions serrées avec les cellules adjacentes, les espaces intercellulaires de la couche cellulaire sont occlus et le flux de courant est restreint [16]. Ceci induit une résistance plus élevée au courant, ce qui se reflète dans des valeurs de TEER plus élevées. La TEER est souvent exprimée normalisée à la surface de la membrane dans l'unité Ωcm2, comme indiqué ci-dessous, pour faciliter la comparaison directe avec d'autres modèles.
𝑇𝐸𝐸𝑅 (Ω 𝑐𝑚2) = 𝑅𝑒𝑠𝑖𝑠𝑡𝑎𝑛𝑐𝑒 (Ω) × 𝐶𝑒𝑙𝑙 𝑐𝑢𝑙𝑡𝑢𝑟𝑒 𝑎𝑟𝑒𝑎 (𝑐𝑚2)
Dans les modèles de BHE sur puce, la mesure de la TEER est une méthode rapide et non invasive permettant une évaluation en temps réel de la qualité de la barrière. Les mesures sont effectuées en appliquant un faible courant électrique à travers la couche cellulaire tout en mesurant l'impédance du courant par la couche cellulaire. Les dispositifs organe-sur-puce sont adaptés à l'intégration de capteurs où la TEER peut être surveillée en temps réel, ce qui est difficile avec d'autres types de dispositifs. Les modèles in vitro de la BHE doivent atteindre des valeurs de TEER supérieures à 150-200 Ωcm2 pour être considérés comme des modèles acceptables [19]. Ceci est environ dix fois inférieur aux résultats rapportés in vivo . La raison pour laquelle une TEER beaucoup plus faible est acceptée est due aux conditions simplifiées in vitro.
Perméabilité des modèles de barrière hémato-encéphalique sur puce
Les modèles organe-sur-puce peuvent fournir directement des informations sur la fonction de barrière en testant la perméabilité de la barrière à différentes substances. Il est utile de quantifier la perméabilité de manière à ce qu'elle puisse être facilement comparée aux données in vivo. Le transport passif à travers la barrière peut être quantifié à partir du coefficient de perméabilité d'un analyte s'écoulant à travers la puce. Il convient de noter que des facteurs autres que la diffusion peuvent contribuer au transport, tels que le flux convectif s'il y a des lacunes dans la barrière cellulaire, et le flux osmotique dû aux différences de concentrations de solutés entre les canaux. Ceci peut être évité en contrôlant la concentration du soluté dans les canaux et en ayant la même pression dans les deux canaux pendant les expériences. Le transport des composés hydrophiles à travers la barrière étant très restreint, ces composés marqués par des traceurs fluorescents sont souvent utilisés pour les études de perméabilité. La perméabilité peut ensuite être visualisée à l'aide d'un microscope à fluorescence.
Rédigé par Emma Thomée, doctorante pour le projet MAMI, avec le financement du programme de recherche et d'innovation Horizon 2020 de l'Union européenne, au titre de la convention de subvention n° 766007.
Bibliographie
- Abbott, N.J., et al., Structure and function of the blood-brain barrier. Neurobiol Dis, 2010. 37(1): p. 13-25.
- Wong, A.D., et al., La barrière hémato-encéphalique : une perspective d'ingénierie. Front Neuroeng, 2013. 6: p. 7.
- Bhatia, S.N. et D.E. Ingber, Organes sur puce microfluidiques. Nat Biotechnol, 2014. 32(8): p. 760-72.
- Booth, R. et H. Kim, Characterization of a microfluidic in vitro model of the blood-brain barrier ([small mu ]BBB). Lab on a Chip, 2012. 12(10): p. 1784-1792.
- Booth, R. et H. Kim, Analyse de la perméabilité des médicaments neuroactifs à travers un modèle dynamique de barrière hémato-encéphalique in vitro microfluidique. Ann Biomed Eng, 2014. 42(12): p. 2379-91.
- Griep, L.M., et al., BBB on chip: microfluidic platform to mechanically and biochemically modulate blood-brain barrier function. Biomed Microdevices, 2013. 15(1): p. 145-50.
- Sia, S.K. et G.M. Whitesides, Dispositifs microfluidiques fabriqués en poly(diméthylsiloxane) pour les études biologiques. Electrophoresis, 2003. 24(21): p. 3563-76.
- Hawkins, B.T. et T.P. Davis, The Blood-Brain Barrier/Neurovascular Unit in Health and Disease. Pharmacological Reviews, 2005. 57(2): p. 173.
- Pamies, D., T. Hartung, et H.T. Hogberg, Biological and medical applications of a brain-on-a-chip. Experimental Biology and Medicine, 2014. 239(9): p. 1096-1107.
- Serlin, Y., et al., Anatomie et physiologie de la barrière hémato-encéphalique. Seminars in cell & developmental biology, 2015. 38: p. 2-6.
- Bang, S., et al., Une plateforme microfluidique de barrière hémato-encéphalique à faible perméabilité avec contact direct entre le réseau vasculaire perfusable et les astrocytes. Scientific Reports, 2017. 7(1): p. 8083.
- Adriani, G., et al., A 3D neurovascular microfluidic model consisting of neurons, astrocytes and cerebral endothelial cells as a blood-brain barrier. Lab On A Chip, 2017. 17(3): p. 448-459.
- Dewey, C.F., et al., The dynamic response of vascular endothelial cells to fluid shear stress. J Biomech Eng, 1981. 103(3): p. 177-85.
- van der Helm, M.W., et al.,Technologie microfluidique d'organe sur puce pour la recherche sur la barrière hémato-encéphalique.Tissue Barriers, 2016.4(1) : p. e1142493.
- Srinivasan, B., et al., TEER measurement techniques for in vitro barrier model systems. J Lab Autom, 2015. 20(2): p. 107-26.
- Thuenauer, R., E. Rodriguez-Boulan, et W. Römer, Approches microfluidiques pour la culture et la caractérisation de couches de cellules épithéliales. Analyst, 2014. 139(13): p. 3206-18.
- Benson, K., S. Cramer, et H.J. Galla, Surveillance cellulaire basée sur l'impédance : propriétés de barrière et au-delà. Fluids Barriers CNS, 2013. 10(1): p. 5.
- Wegener, J. et J. Seebach, Outils expérimentaux pour surveiller la dynamique de la fonction de barrière endothéliale : une revue des approches in vitro. Cell Tissue Res, 2014. 355(3): p. 485-514.
- Reichel, A., D.J. Begley, and N.J. Abbott, An overview of in vitro techniques for blood-brain barrier studies. Methods Mol Med, 2003. 89: p. 307-24.