Alors que le développement des dispositifs microfluidiques, tels que les puces de culture cellulaire et les organes sur puce, continue de croître, la stérilisation devient une étape critique pour maintenir l'intégrité de ces systèmes. Tout équipement entrant en contact avec des fluides biologiques sensibles doit être soigneusement stérilisé pour garantir la viabilité et la reproductibilité des résultats expérimentaux. Bien que plusieurs méthodes de stérilisation existent, l'autoclavage (ou stérilisation à la vapeur) reste le choix le plus populaire en raison de son efficacité, de sa simplicité, de son faible coût et de sa nature respectueuse de l'environnement, ne produisant aucun résidu toxique.
Cette revue présente les différents types d'autoclaves, discute de leurs mécanismes et identifie les matériaux les plus compatibles avec cette méthode de stérilisation.
Comment fonctionne un autoclave pour la stérilisation ?
L'autoclavage repose sur la stérilisation par la chaleur, un processus simple qui implique l'exposition des dispositifs à de la vapeur saturée à 121 °C pendant 20 minutes sous une pression de 115 kPa. La chaleur élevée provoque la dénaturation des protéines, perturbant efficacement les activités microbiennes et assurant la stérilisation. Cependant, si les conditions ne sont pas optimales, l'activité microbienne peut s'arrêter temporairement mais reprendre une fois que la température baisse.
Pour une destruction efficace des germes, la vapeur utilisée doit être homogène et saturée, la haute température générant une pression correspondante, comme le dicte la loi de Regnault. Il est essentiel d'utiliser de l'eau déminéralisée pour produire de la vapeur, car cela empêche toute substance en suspension de contaminer le système.
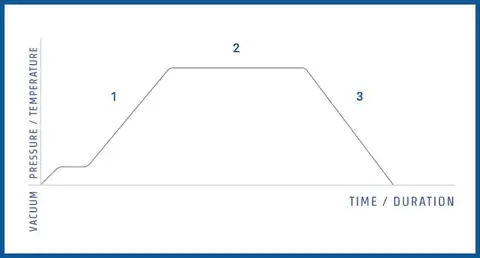
Un cycle d'autoclavage typique (tel que celui représenté dans la figure ci-dessous) comprend :
- Pre-sterilization phase: Multiple steam injections alternate with vacuum injections to purge air from the sterilization chamber. The absence of air ensures better steam penetration.
- Phase de stérilisation : La chambre est maintenue à une température et une pression cibles pendant une durée déterminée (par exemple, 121°C pendant 20 minutes).
- Phase de refroidissement : Après la stérilisation, la chambre refroidit et la pression diminue jusqu'à atteindre les niveaux atmosphériques.
Différents types d'autoclaves
Les autoclaves sont classés en trois types principaux : Classe N, Classe B et Classe S. Comprendre leurs différences est essentiel pour choisir le meilleur autoclave pour des applications spécifiques, notamment en microfluidique.
Autoclave de Classe N
The Class N autoclave is designed for simple solid products (referred to as "naked solid products") and cannot effectively sterilize textiles, porous materials, hollow items, or products in sealed containers. A notable limitation is its inconsistent steam penetration, primarily because it does not require vacuum pre-conditioning. As a result, Class N autoclaves are best suited for straightforward, non-porous materials.
Autoclave de Classe B
Les autoclaves de Classe B, également connus sous le nom de « grands petits stérilisateurs », sont compacts mais très efficaces, capables de stériliser une large gamme de matériaux. Cela inclut les matériaux poreux, les textiles, les objets creux comme les seringues en verre, et les produits scellés. La norme EN 13060 définit leurs performances et leurs cycles, ce qui en fait un choix fiable pour les applications médicales et microfluidiques. Leur polyvalence et leur petite taille en font l'option privilégiée pour la microfluidique.
Autoclave de Classe S
Les autoclaves de Classe S se situent entre la Classe N et la Classe B en termes de fonctionnalité. Ces machines varient considérablement en termes de performances car elles ne sont pas soumises à une norme spécifique, leurs capacités de stérilisation étant déterminées par le fabricant. De ce fait, elles sont moins couramment utilisées pour des applications précises comme la microfluidique.
Choisir le bon autoclave pour la microfluidique
Given the sensitive nature of materials and devices used in microfluidics, the Class B autoclave emerges as the most appropriate choice. Its versatility, capacity to handle a wide variety of materials (including porous and hollow items), and adherence to strict safety standards make it well-suited for microfluidic sterilization processes.
Autoclavable Materials in Microfluidics
Determining which materials can withstand the high temperatures (121°C) and pressures used in autoclaving without suffering damage is a significant challenge in microfluidics. While many common microfluidic materials are autoclavable, several others, such as PMMA, PVC, and PC, are often mistakenly assumed to be suitable for autoclaving when they are not. This is due to their glass transition temperatures (Tg) being below 121°C, which means these materials could potentially melt or deform during the process. Therefore, it is essential to verify the thermal properties of each material before sterilization to avoid damage.
To ensure the efficiency and safety of your microfluidic system, refer to the table below for informed decisions about which materials are truly autoclavable.
Additionally, always consult the manufacturer’s instructions for specific guidance on the compatibility of individual components—whether you are working with tubing, chips, or connectors—before proceeding with any sterilization procedure.
| Matériau | Autoclavable ? |
|---|---|
| Acier inoxydable 316 | Oui |
| Acrylique | Oui |
| Verre borosilicaté | Oui |
| Delrin (Polyoxyméthylène) | Oui |
| ETFE (Ethylene Tetrafluoroethylene) | Oui |
| FEP (Éthylène-Propylène Fluoré) | Oui |
| Halar | Oui |
| High Purity PFA | Oui |
| Nylon | Non |
| PC (Polycarbonate) | Non |
| PCTFE (Polychlorotrifluoroéthylène) | Oui |
| PDMS (Polydiméthylsiloxane) | Oui |
| PEEK (Polyetheretherketone) | Oui |
| Perlast | Oui |
| PFA (Perfluoroalkoxy) | Oui |
| PK (Polycétone) | Oui |
| PMMA (Polyméthacrylate de méthyle) | Non |
| PE (Polyéthylène) | Non |
| Polysulfone | Oui |
| PP (Polypropylène) | Oui |
| PPS (Sulfure de Polyphénylène) | Oui |
| PS (Polystyrène) | Non |
| PTFE (Polytetrafluoroethylene) | Oui |
| PVC (Polychlorure de vinyle) | Non |
| Radel® | Oui |
| Silicone | Oui |
| Verre sodo-calcique | Non |
| Titane | Oui |
| Topas - COC (Copolymère d'oléfine cyclique) | Non |
| TPX® (Polyméthylpentène) | Oui |
| UHMWPE (Polyéthylène à très haut poids moléculaire) | Non |
| Ultem | Oui |
| Vespel | Oui |
| Zeonex - COP (Polymère d'Oléfine Cyclique) | Non |
| Zeonor - COP (Polymère d'Oléfine Cyclique) | Non |
Conclusion
La stérilisation est une étape cruciale en microfluidique, particulièrement pour les applications biomédicales et biologiques. La stérilisation à la vapeur par autoclavage est une méthode fiable et largement employée, à condition que les protocoles adéquats soient respectés. En sélectionnant des autoclaves appropriés — tels que les autoclaves de Classe B — et en garantissant la compatibilité des matériaux, vous pouvez assurer la sécurité et la performance de vos dispositifs microfluidiques.
Restez à l'écoute pour plus d'informations, de tutoriels et d'applications pratiques dans nos futurs articles. D'ici là, soyez courageux, autoclavez, ne laissez pas les microbes se mal comporter 🧪🔬!
📧 If you have any questions or feedback, please feel free to contact us at support@darwin-microfluidics.com.


