Le foie joue un rôle fondamental dans les activités métaboliques telles que la régulation des niveaux de glucose dans le sang, la production de protéines plasmatiques, le métabolisme des médicaments, la production de bile [1][2] et présente une structure complexe d'un point de vue morphologique et fonctionnel [3].
En raison de son importance, il a été largement étudié au cours des dernières décennies afin de comprendre les mécanismes du métabolisme et de la toxicité des médicaments (DILI – Lésion hépatique d'origine médicamenteuse) ainsi que les maladies hépatiques telles que l'hépatite, la cirrhose, la fibrose et les cancers [4][5][6].
Bref aperçu de la structure du sinusoïde hépatique
La veine porte hépatique (provenant de l'intestin) et l'artère hépatique acheminent le sang vers le foie, où il est mélangé dans des capillaires appelés sinusoïdes et collecté dans la veine hépatique centrale, où il est ramené au cœur.
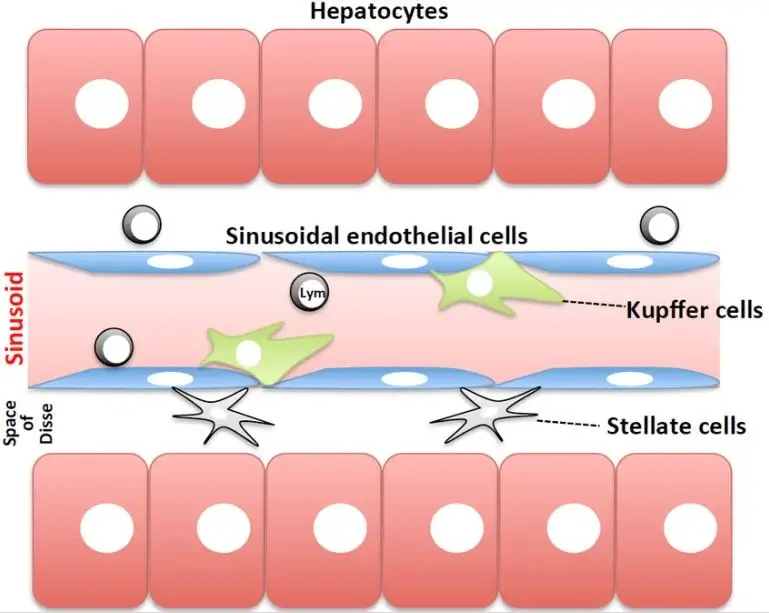
Le foie est composé d'unités répétitives, les lobules, de forme hexagonale, qui sont constitués d'hépatocytes (HCs) agencés en structures cordées autour des sinusoïdes, séparés par un espace périsinusoïdal, l'espace de Disse.
Les hépatocytes sont les cellules parenchymateuses du foie, principalement impliquées dans la synthèse des protéines et de la bile, ainsi que dans le métabolisme hépatique, tandis que les principales cellules non parenchymateuses (NPC) sont les cellules endothéliales sinusoïdales hépatiques (LSEC), les cellules de Kupffer (macrophages) et les cellules étoilées. Les hépatocytes reçoivent les nutriments des cellules sinusoïdales par des échanges à travers l'espace de Disse [2] [7][8].
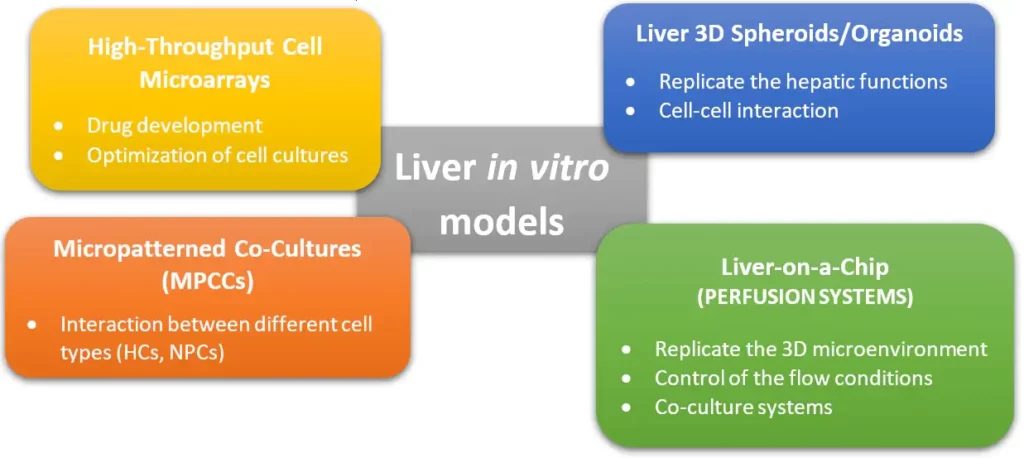
Modèles de foie in vitro d'ingénierie
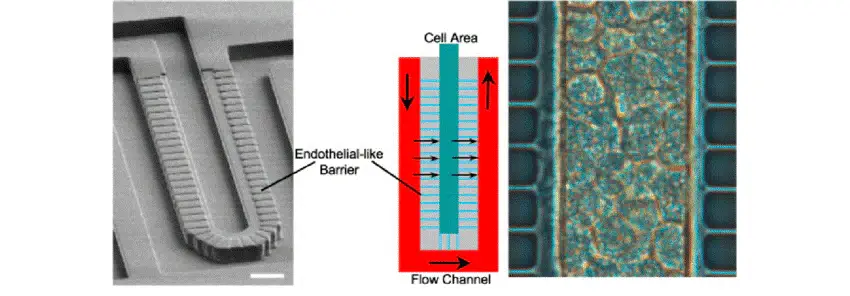
A liver-on-a-chip model: The artifical liver sinusoid
Nous avons choisi de décrire ici le sinusoïde hépatique artificiel développé par Lee et al., qui ont conçu une plateforme microfluidique capable de recréer un microenvironnement physiologique (conditions de transport de masse) pour l'ensemencement d'hépatocytes primaires [11].
Details on chip design
The microfluidic platform was composed of a channel for the flow of nutrients and drugs and a cell compartment for the seeding of tightly packed hepatocytes.
En effet, il a été démontré que des densités élevées de cellules primaires permettent la formation d'interactions cellule-cellule avec une viabilité et une activité métabolique accrues.
A permeable endothelial-like barrier with a sinusoidal shape composed of a set of parallel microchannels was included into the chip design in order to (i) prevent high shear stresses that can be dangerous for the HCs and (ii) pack the HCs in the cell area.
How to make a liver on a chip?
Chip microfabrication
SU-8 (a negative photoresist) was patterned through photolithography on a silicon wafer in two steps: a 1 µm thick SU-8 layer was spin-coated to create the channels of the endothelial-like barrier, then a 30 µm SU-8 was used to create the channels for the flow and the cells seeding.
Successively, poly-dimethyl siloxane (PDMS) chips were replicated from the SU-8 mold and bonded to a glass slide.
Designing the chip parameters to mimic the liver microcirculation
The chip was designed to ensure a nutrient volumetric flow of 100 pL/s (for about 250 hepatocytes loaded in the cell area), typical of liver microcirculation. To do so, the channels width, height and length were set at (50 x 30 x 1200) µm and (2 x 1 x 30) µm for the flow channel and the permeable barrier respectively.
Using a barrier channels cross-section of 2 x 1 µm, a low convective flow, so a high total fluidic resistance (1000 times higher than in the fluid channel) were ensured, thus enabling diffusive transport. In this way, HCs were exposed to low shear stresses and could receive nutrients through diffusion across the barrier.
Designing the chip parameters to control the loading of tightly packed hepatocytes
La conception de la barrière de type endothélial a également permis le chargement d'une densité élevée de HCs sans les endommager ni la barrière elle-même.
La section transversale étroite des canaux a été vérifiée pour réduire la déformation de la membrane cellulaire à l'interface.
Ainsi, un flux positif a dirigé les cellules vers le bas de la zone cellulaire sans colmatage, ce qui a entraîné une forte compaction des cellules. De plus, une résistance croissante produite par les cellules a déterminé une diminution du taux de chargement à la fin du processus d'ensemencement.
Microfluidic chip for primary cells culture: Results and conclusion
Des hépatocytes primaires de rat et humains ont été chargés dans la zone cellulaire et la viabilité cellulaire a été évaluée jusqu'à 7 jours.
La plateforme microfluidique a été perfusée en continu avec du milieu de culture. Les résultats ont montré que les deux lignées cellulaires ont maintenu leur viabilité après 7 jours sans nécessiter de revêtement de collagène (nécessaire dans les systèmes de culture statiques).
De plus, la haute densité cellulaire assurait une activité métabolique élevée grâce aux contacts cellule-cellule.
The review shows how microfluidic platforms can be engineered to closely mimic specific functions of a tissue or an organ. In this work, a microfluidic device composed of a flow channel, a cell area and a permeable endothelial-like barrier was designed to resemble the liver microcirculation conditions, improving the hepatocytes viability and the cell-cell interactions.
Review written by Alessandra Dellaquila.
Références
[1] Y. B. Kang et al., “Liver sinusoid on a chip: Long‐term layered co‐culture of primary rat hepatocytes and endothelial cells in microfluidic platforms,” Biotechnol. Bioeng., vol. 112, no. 12, pp. 2571–2582, 2015.
[2] C. H. Beckwitt et al., “liver ‘organ on a chip,’” Exp. Cell Res., 2017.
[3] Y. Du et al., “Mimicking liver sinusoidal structures and functions using a 3D-configured microfluidic chip,” Lab Chip, vol. 17, no. 5, pp. 782–794, 2017.
[4] L. A. Vernetti et al., “A human liver microphysiology platform for investigating physiology, drug safety, and disease models,” Exp. Biol. Med., vol. 241, no. 1, pp. 101–114, 2016.
[5] V. Natarajan, E. N. Harris, and S. Kidambi, “CEsS (cellules endothéliales sinusoïdales), microenvironnement hépatique et fibrose,” Biomed Res. Int., vol. 2017, 2017.
[6] S. S. Bale et al., “Plateformes in vitro pour l'évaluation de la toxicité hépatique,” Exp. Biol. Med., vol. 239, no. 9, pp. 1180–1191, 2014.
[7] A. J. Strain and J. M. Neuberger, “Un foie bioartificiel – état de l'art,” Science (80-. )., vol. 295, no. 5557, pp. 1005–1009, 2002.
[8] C. Moraes, G. Mehta, S. C. Lesher-Perez, and S. Takayama, Organs-on-a-Chip: A Focus on Compartmentalized Microdevices, vol. 40. 2011.
[9] H. Tsutsui and S. Nishiguchi, Importance des cellules de Kupffer dans le développement des lésions hépatiques aiguës chez la souris, vol. 15. 2014.
[10] G. H. Underhill et S. R. Khetani, “Bioengineered Liver Models for Drug Testing and Cell Differentiation Studies,” Cell. Mol. Gastroenterol. Hepatol., vol. 5, no. 3, pp. 426–439, 2018.
[11] P. J. Lee, P. J. Hung et L. P. Lee, “An artificial liver sinusoid with a microfluidic endothelial‐like barrier for primary hepatocyte culture,” Biotechnol. Bioeng., vol. 97, no. 5, pp. 1340–1346, 2007.