Chacune de ces techniques présente des avantages et des inconvénients, et le choix dépendra de l'application microfluidique. En fin de compte, mesurer précisément la contrainte de cisaillement peut aider les scientifiques à mieux comprendre le comportement cellulaire dans des conditions d'écoulement.
Quelle est la définition de la contrainte de cisaillement ?
La contrainte de cisaillement est définie comme la contrainte créée lorsqu'une force tangentielle agit sur une surface. La définition de la contrainte de cisaillement appliquée à la biologie et à la microfluidique est la force de frottement d'un flux de fluide biologique agissant sur les cellules ou les tissus.Comment déterminer la contrainte de cisaillement ?
La contrainte de cisaillement du fluide augmente avec la vitesse du fluide et avec la viscosité ; par conséquent, pour les fluides newtoniens, elle peut être calculée selon la loi de Newton avec la relation suivante^{1}:\tau =\eta \frac{\partial v}{\partial z}
où \eta la viscosité est la viscosité (g/cm-s = Poise)\frac{\partial v}{\partial z} est le gradient de vitesse ou le taux de cisaillement (s^{-1}), Dans le système SI, l'unité est le Pascal (Pa), mais dans le système cardiovasculaire, une autre unité est souvent utilisée : dyn/cm2 (1 Pa = 10 dyn/cm2).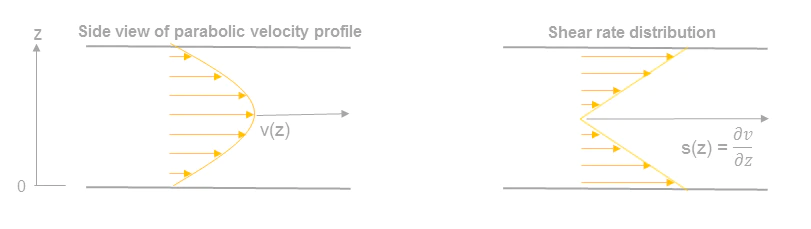
Le flux de fluide n'a pas la même vitesse en tout point du canal, créant une distribution de vitesse avec un profil de vitesse qui tend à être parabolique dans la plupart des cas simples d'écoulement laminaire. La vitesse du fluide est la plus rapide au centre et la plus lente près de la paroi du canal. Lorsque z=0, la contrainte de cisaillement créée par le fluide est appelée « contrainte de cisaillement pariétale » et le gradient de vitesse est généralement appelé « taux de cisaillement pariétal ». L'ordre de grandeur de la contrainte de cisaillement pariétale est généralement la valeur la plus élevée dans le canal. Lors d'expériences avec des cellules adhérentes ou pour éviter les effets néfastes de la contrainte de cisaillement, la valeur de la contrainte de cisaillement pariétale est généralement celle utilisée.
Lors de la mise en place d'une expérience de biologie en microfluidique, il est crucial de prendre en compte la contrainte de cisaillement. L'objectif final peut être soit d'éviter la contrainte de cisaillement et de la réduire à sa valeur minimale pour prévenir la détérioration, voire la mort cellulaire, soit de mimer la contrainte de cisaillement in vivo pour étudier des processus physiologiques tels que l'impact des contraintes mécaniques sur les cellules.
Afin de reproduire un processus biologique, il est important de savoir ce qui se passe in vivo. De nombreux articles ont décrit ce phénomène et ses conséquences in vivo.
Contrainte de cisaillement in vivo
Wherever there is flow, shear stress exists. In vivo, shear stress is mostly due to the frictional force of blood flow against the vessel walls. In our body, some cells are continuously under shear stresses such as endothelial cells and kidney epithelial cells but flow patterns are not uniform in the vascular system^{2}:
- Dans les veines et les petites artères : Un écoulement généralement laminaire et des contraintes de cisaillement pariétales élevées sont principalement observés.
- Dans les ramifications et les courbures : Modèle d'écoulement perturbé & Faible contrainte de cisaillement pariétal
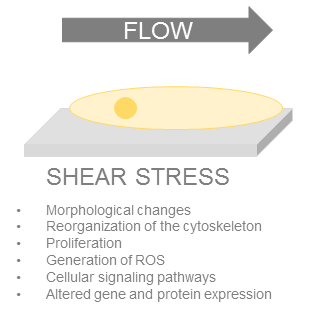
Les forces hémodynamiques et la contrainte mécanique résultante entraînent de nombreuses réponses biologiques qui ont été bien identifiées au cours des dernières décennies. Le premier impact observable est un changement de morphologie, les cellules s'allongeant dans la direction de l'écoulement. Après exposition à la contrainte de cisaillement, on observe également une réorganisation claire du cytosquelette^{3}, l'alignement des microtubules et un changement de la distribution de l'actine.
Par exemple, il a été démontré que les contraintes de cisaillement altèrent l'expression génique, régulent l'activation des voies de signalisation et ont un certain impact sur l'absorption de calcium, la différenciation, la prolifération et l'expression des protéines. Lorsque la contrainte de cisaillement augmente, les mécanismes de prolifération sont activés.
De plus, les processus de remodelage vasculaire peuvent être observés avec une expansion du diamètre du vaisseau et une augmentation de l'épaisseur de la paroi^{4}. Au contraire, de faibles valeurs de contrainte de cisaillement entraîneront une réduction du diamètre du vaisseau.
Le comportement cellulaire sous contrainte de cisaillement a été décrit dans de nombreux articles. Selon la lignée cellulaire, l'impact peut être différent. Pour les cellules souches, cela peut induire une différenciation, et pour les cellules endothéliales (CE), la contrainte de cisaillement a un impact considérable sur le phénotype et peut même entraîner certaines pathologies.
Par exemple, dans les régions soumises à un cisaillement oscillant, cela peut entraîner des modifications pathologiques des parois artérielles et augmenter le risque d'athérosclérose^{5}. L'altération du cisaillement peut également jouer un rôle dans les anévrismes en raison de la synthèse d'espèces réactives de l'oxygène (ROS), d'oxyde nitrique (NO), de facteurs de croissance et de métalloprotéinases.
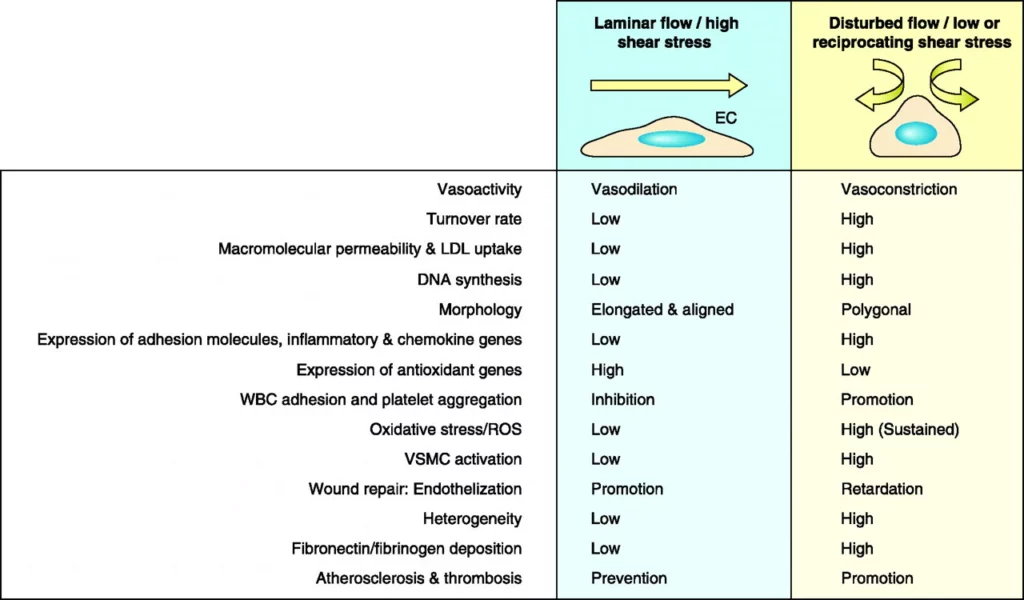
La contrainte de cisaillement joue un rôle important dans divers processus biologiques aux niveaux moléculaire et clinique. Les forces mécaniques sont détectées par les cellules, ce qui conduit à une mécanotransduction en réponses biologiques. Ci-dessous, un résumé des différents effets décrits dans la littérature en fonction du profil d'écoulement et de la contrainte de cisaillement :
Les valeurs moyennes de contrainte de cisaillement dans les artères humaines en conditions basales sont d'environ 2 à 20 dyne/cm². Il est important de souligner que même à une contrainte de cisaillement aussi faible que 4 dyne/cm², des changements morphologiques sont observés in vivo. Des valeurs beaucoup plus élevées^{6} (de 30 à 100 dyne/cm²) peuvent être observées près des branches artérielles et des fortes courbures telles que la crosse aortique, les bifurcations, tandis que des valeurs beaucoup plus faibles, de 1 à 6 dyne/cm², sont généralement mesurées dans les veines.
Contrainte de cisaillement in vitro
Dans les cultures cellulaires 2D conventionnelles, les cellules ne sont pas exposées à des forces mécaniques telles que la contrainte de cisaillement, la tension et la compression, qui ont un impact sur le développement et la fonction des organes.
Par exemple, en l'absence de flux de fluide, l'interaction entre les cellules étudiées et les cellules sanguines et immunitaires ne peut pas être évaluée. C'est une énorme limitation des études de culture cellulaire.
Par conséquent, l'utilisation de dispositifs microfluidiques constitue une alternative viable aux techniques in vitro traditionnelles en raison de sa pertinence physiologique. La microfluidique peut fournir un microenvironnement biomimétique 3D et, plus récemment, elle est même utilisée pour créer des organes sur puce afin de mimer des organes in vitro. Ces applications sont plus proches de ce qui se passe in vivo, mais le nouveau défi consiste à prendre en compte les forces mécaniques telles que la contrainte de cisaillement.
Dans les dispositifs microfluidiques, la contrainte de cisaillement est créée par l'injection du flux de fluide. En raison des petites dimensions des dispositifs microfluidiques, l'écoulement est laminaire ; par conséquent, c'est un bon moyen de mimer les écoulements trouvés dans les veines et les petites artères où l'écoulement est généralement unidirectionnel et laminaire^{7}. Dans les artères plus grandes, les écoulements rencontrés sont souvent pulsatiles et laminaires. Dans une expérience microfluidique, le débit peut être modifié périodiquement pour mimer ce type d'écoulement.
En général, la plupart des profils d'écoulement peuvent être mimés avec la microfluidique, la seule exception étant l'écoulement turbulent, rarement rencontré dans les systèmes biologiques. L'expérimentation microfluidique constitue donc une bonne approximation in-vivo^{8}. D'autre part, la contrainte de cisaillement peut également être perçue comme un inconvénient en raison des effets néfastes inhérents observés à des niveaux élevés. Heureusement, il est possible de concevoir une expérience microfluidique de manière à ce que la contrainte de cisaillement n'ait pas d'effets indésirables.
Dans les deux situations : investigation de phénomènes biologiques ou lorsque la contrainte de cisaillement est considérée comme un facteur limitant, il est crucial de prendre le temps et de prendre en compte certains paramètres lors de la conception de l'expérience.
Microfluidique et contrainte de cisaillement dans les expériences cellulaires
Parmi tous les éléments à prendre en compte lors de la conception d'une expérience microfluidique, le niveau de contrainte de cisaillement subi par les cellules est une préoccupation physiologiquement importante. Dans les dispositifs microfluidiques, plusieurs paramètres influenceront la contrainte de cisaillement : les dimensions et la géométrie des canaux, la concentration cellulaire, le type de lignée cellulaire, la manière dont le débit est délivré, etc. Certains des paramètres mentionnés seront décrits plus en détail afin de comprendre comment contrôler et mesurer la contrainte de cisaillement dans les dispositifs microfluidiques.
Conception d'une expérience microfluidique
Mimer la contrainte de cisaillement in vivo : valeurs expérimentales
Dans les expériences où des conditions statiques et biomimétiques sont souhaitées, la valeur utilisée est comprise entre : 0,2 et 0,5 dyne/cm². Afin d'imiter l'écoulement à travers un certain type de vaisseau, les valeurs indiquées de contraintes de cisaillement et de taux de cisaillement ci-dessous peuvent être utilisées comme référence :
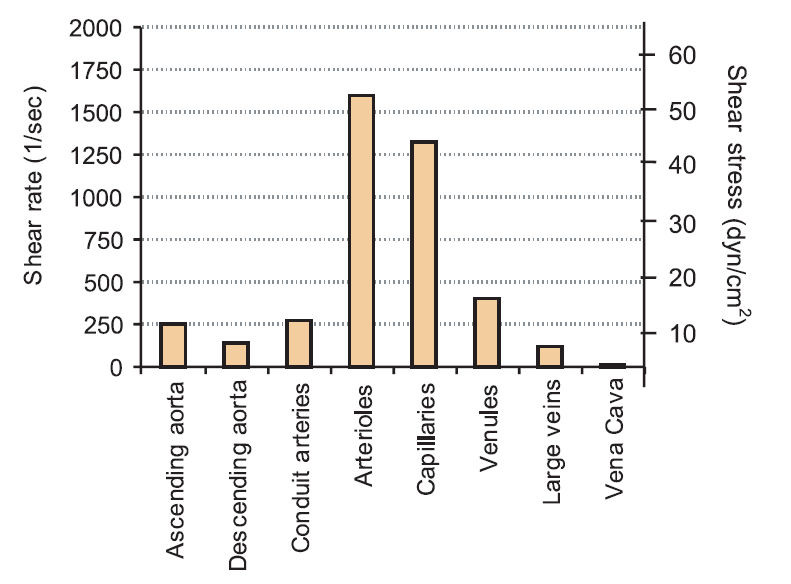
Choix des lignées cellulaires
Les réponses cellulaires à la contrainte de cisaillement et leur capacité à résister aux forces du fluide dépendent des types de cellules. Dans certaines études, différents types de cellules ont été observés dans les mêmes conditions, ce qui a conduit à la conclusion qu'il existe un large éventail de réponses à la contrainte de cisaillement selon la cellule utilisée. Une étape de la conception de l'expérience consiste à déterminer quelles lignées cellulaires doivent être utilisées et quel débit doit être appliqué en fonction du résultat souhaité.
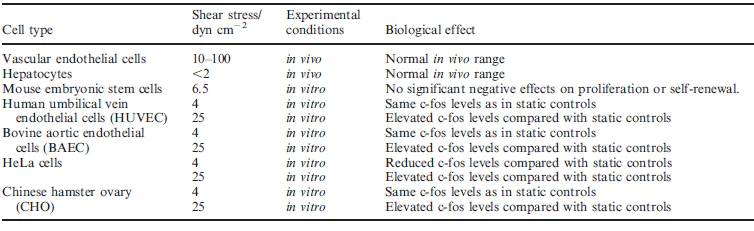
Conception de puces
Dans tout système fluidique, la capacité à prédire la contrainte de cisaillement est d'une grande importance pour prédire les conséquences sur le phénotype des cellules^{11}. Ainsi, lors de la conception d'une expérience et d'une nouvelle puce microfluidique, la contrainte de cisaillement peut être calculée ou modélisée.
Choix du système de contrôle de flux
En microfluidique et dans les expériences cellulaires, il est crucial d'obtenir un contrôle de flux précis et fluide. C'est un paramètre clé pour contrôler la contrainte de cisaillement et, par conséquent, le choix de l'instrument de contrôle de flux est important.
Plusieurs options existent, telles que les pousse-seringues, les pompes péristaltiques, ou les systèmes de contrôle de pression avec ou sans commutateurs de débit. Chacun de ces systèmes présente des avantages et des inconvénients, et le choix dépendra de l'application microfluidique. L'article suivant détaille davantage les avantages et inconvénients relatifs des méthodes populaires de contrôle de débit.
Lorsqu'il s'agit de la contrainte de cisaillement, il y a des inconvénients majeurs à éviter : un temps de réponse lent, des oscillations de débit indésirables et des fluctuations incontrôlables. Ces inconvénients peuvent entraîner une différence majeure entre le débit calculé/simulé et le débit réel. Afin d'obtenir un débit aussi proche que souhaité, un temps de réponse rapide et un contrôle précis du débit, un système de contrôle de pression peut être l'une des meilleures solutions sur le marché.
Comment mesurer la contrainte de cisaillement ?
L'évaluation de la contrainte de cisaillement dans une culture cellulaire sous écoulement peut être réalisée de plusieurs manières. La contrainte de cisaillement peut être évaluée à l'aide de méthodes théoriques et numériques de la dynamique des fluides. Afin de calculer l'écoulement, et par conséquent la contrainte de cisaillement, dans une configuration microfluidique, il est nécessaire de résoudre l'équation de Navier-Stokes, numériquement ou analytiquement, pour déterminer le profil de vitesse de la géométrie considérée. Dans le cas de géométries simples, telles qu'un canal rectangulaire large ou un canal tubulaire, la solution analytique est simple et peut être trouvée dans la littérature. Par exemple, pour un canal rectangulaire de dimensions w*h*l avec h>w>>l, la contrainte de cisaillement pariétale peut être calculée comme \tau=\frac{6\eta Q}{h²W} où Q est le débit. Pour un canal cylindrique, la contrainte de cisaillement est \tau=\frac{4\eta Q}{R^{3}}/\pi.
Cependant, ces formules simples ne représentent pas la contrainte de cisaillement pour des géométries complexes où il est généralement préférable d'effectuer une simulation informatique pour estimer la contrainte ou le taux de cisaillement.
Ces calculs sont très utiles pour estimer, voire déterminer avec précision, la contrainte de cisaillement. Cependant, lorsqu'il s'agit de déterminer expérimentalement la contrainte de cisaillement avec la plus grande exactitude possible dans une expérience microfluidique, plusieurs méthodes permettant une mesure ou une estimation locale de la contrainte de cisaillement dans la région d'intérêt peuvent être employées. Nous avons développé un outil simple (mais pratique) pour vous aider à déterminer la pression approximative dans votre puce.
Pour l'investigation dans les cultures cellulaires, il peut être souhaitable de mesurer la contrainte de cisaillement aussi près que possible des cellules. Il existe plusieurs méthodes de détection pour ce faire.
Capteur à base de cellules
Les contraintes de cisaillement de flux peuvent entraîner l'activation de certaines voies de signalisation^{12}. Une méthode développée pour mesurer la contrainte de cisaillement est l'utilisation de capteurs cellulaires fluorescents génétiquement encodés réagissant à l'activation de la voie de contrainte de cisaillement de flux.
Cristal liquide
L'utilisation potentielle des cristaux liquides comme technique de mesure du cisaillement a été démontrée dans les dispositifs microfluidiques^{13}. Cette technique expérimentale repose sur les propriétés des cristaux liquides et leurs structures moléculaires chirales. Lorsqu'une contrainte de cisaillement est appliquée, la structure des molécules se déforme, ce qui peut entraîner un changement de polarisation ou de longueur d'onde mesurable.
Micro-vélocimétrie par particules
Les systèmes de micro-vélocimétrie par particules (µ-PIV) peuvent être utilisés pour obtenir une lecture précise de la contrainte de cisaillement pariétale qui peut également résoudre directement la surface des cellules^{14}. Cela permet de mesurer le profil d'écoulement pour déterminer la contrainte de cisaillement. Un système µ-PIV se compose d'une caméra haute vitesse synchronisée avec un laser à double cavité qui illumine les particules introduites dans le flux de fluide et surveille leur position avec une grande précision. De tels systèmes sont très puissants, mais la complexité de leur mise en œuvre les rend inadaptés à une mesure facile de la contrainte de cisaillement.
Vélocimétrie Doppler Laser
Une autre façon de mesurer les profils de vitesse dans les écoulements liquides près de l'interface est d'utiliser le décalage Doppler de la lumière laser^{15}. Ici, le décalage Doppler d'une lumière laser réfléchie à l'intérieur du flux est surveillé afin de mesurer le profil d'écoulement du liquide et de déterminer la contrainte de cisaillement. L'appareil pour une telle mesure est plus simple que pour la vélocimétrie par image, car le laser n'a pas besoin d'être synchronisé avec une caméra et il suffit de mesurer son décalage de fréquence, mais le processus est moins documenté et les résultats ne sont pas aussi précis.
Néanmoins, cela représente une alternative très prometteuse pour la mesure de débit à faible coût et l'évaluation de la contrainte de cisaillement plus proche des cellules.
Bibliographie
- Transport phenomena, R. B. Bird, W. E. Stewart, and E. N. Lightfoot, John Wiley and Sons, Inc., New York (1960). 780 pages. 11,50 $. (1961). AIChE Journal, 7(2), pp.5J-6J.
- Chiu, J. et Chien, S. (2011). Effets d'un flux perturbé sur l'endothélium vasculaire : Bases physiopathologiques et perspectives cliniques. Physiological Reviews, 91(1), pp.327-387.
- Malek, A., Izumo S. (1996). Mécanisme de changement de forme des cellules endothéliales et de remodelage cytosquelettique en réponse à la contrainte de cisaillement du fluide. J Cell Sci, (Pt 4):713-26.
- Glagov, S., Zarins, C. et Giddens, D. (1994). Hémodynamique, la structure de la paroi artérielle et l'athérosclérose. Atherosclerosis, 109(1-2), p.343.
- Davies, P. (2008). Hemodynamic shear stress and the endothelium in cardiovascular pathophysiology. Nature Clinical Practice Cardiovascular Medicine, 6(1), pp.16-26.
- Dewey, C., Bussolari, S., Gimbrone, M. et Davies, P. (1981). La réponse dynamique des cellules endothéliales vasculaires à la contrainte de cisaillement du fluide. Journal of Biomechanical Engineering, 103(3), p.177.
- Franklin, K. J. (1937). Veins and the nervous system. In “A Monograph on Veins” (K. J. Franklin, ed.), Chapter 10.
- Freund, J., Goetz, J., Hill, K. et Vermot, J. (2012). Écoulements de fluide et forces dans le développement : fonctions, caractéristiques et principes biophysiques. Development, 139(16), pp.3063-3063.
- Papaioannou TG(1), Stefanadis C. (2005) Contrainte de cisaillement de la paroi vasculaire : principes de base et méthodes. Hellenic J Cardiol 46(1):9-15.
- Kim, L., Toh, Y., Voldman, J. et Yu, H. (2007). Un guide pratique pour la culture par perfusion microfluidique de cellules mammaliennes adhérentes. Lab on a Chip, 7(6), p.681.
- Barber, R. et Emerson, D. (2007). Conception optimale de réseaux microfluidiques utilisant des principes d'inspiration biologique. Microfluidics and Nanofluidics, 4(3), pp.179-191.
- Varma, S. et Voldman, J. (2015). Un capteur à base cellulaire de la contrainte de cisaillement du fluide pour la microfluidique. Lab Chip, 15(6), pp.1563-1573.
- Martel, J., Bradford, A. Bruno, (2008). Mesure de la contrainte de cisaillement dans les systèmes microfluidiques : Technique des cristaux liquides. ASME, pp. 2009-2018 ; 10 pages
- Rossi, M., Lindken, R., Hierck, B. P., & Westerweel, J. (2009). Puce microfluidique conique pour l'étude de la réponse biochimique et mécanique au niveau subcellulaire des cellules endothéliales à l'écoulement de cisaillement. Lab on a Chip, 9(10), 1403-1411.
- Campagnolo, L., Nikolić, M., Perchoux, J., Lim, Y. L., Bertling, K., Loubiere, K., … & Bosch, T. (2013). Mesure du profil d'écoulement dans un microcanal utilisant la technique de détection par interférométrie à rétroaction optique. Microfluidics and Nanofluidics, 14(1-2), 113-119.